选择题(本大题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求)
试题详情
化学在能源、航天等领域应用广泛。下列说法错误的是( )
- A、 为了应对能源危机,应大力发展太阳能、氢能、电能和生物质能等新能源
- B、 我国航天工程近年来成就斐然,卫星计算机芯片使用的是高纯度的硅
- C、 四千余年前我国先辈们用谷物酿造出酒和醋,酿造过程中只发生水解反应
- D、 积极开发废电池的综合利用技术,防止其中的重金属盐对土壤和水源造成污染
试题详情
在2.8gFe中加入100mL3mol/L HCl,Fe完全溶解。 代表阿伏加德罗常数的值,下列说法错误的是( )
代表阿伏加德罗常数的值,下列说法错误的是( )
- A、 HCl溶液中
数为
- B、 反应转移的电子数为
- C、
含有的中子数为
- D、 反应生成标准状况下的气体2.24L
试题详情
下列依据热化学方程式得出的结论正确的是( )
- A、 已知:
:
, 则
- B、 已知:
, 则
的燃烧热
- C、 已知:
, 则稀
和稀
完全反应生成
时,放出
热量
- D、 已知:正丁烷
异丁烷
, 则正丁烷比异丁烷稳定
试题详情
王翰《凉州词》中写道“葡萄美酒夜光杯,欲饮琵琶马上催,…”。夜光杯的主要成分为 , 下列说法正确的是( )
, 下列说法正确的是( )
- A、 基态Si原子的价层电子的轨道表示式:

- B、 镁元素属第三周期s区元素,其原子核外电子的运动状态有12种
- C、 水分子间存在氢键,故水很稳定,1000℃以上才会发生分解
- D、 基态氧原子的电子由2p能级跃迁至3p能级时,可通过光谱仪摄取其发射光谱
试题详情
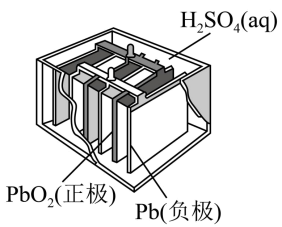
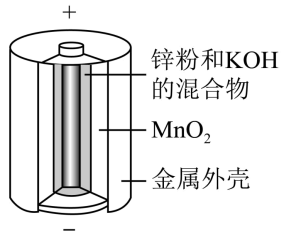
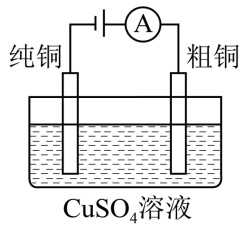
有关下列四个常用电化学装置的叙述中,错误的是( )
|
|
|
|
图1 铅-硫酸蓄电池 | 图2 碱性锌锰电池 | 图3 锌银纽扣电池 | 图4 电解精炼铜 |
- A、 图1所示电池放电过程中,硫酸浓度不断减小
- B、 图2所示电池中,
参加正极反应做氧化剂
- C、 图3所示电池中,
是氧化剂,电池工作过程中被还原为Ag
- D、 图4所示装置工作过程中,电解质溶液中
浓度始终不变
试题详情
下列实验操作正确且能够达到实验目的的是( )
选项 | 实验操作 | 实验目的 |
A | 向某无色溶液中加入铜片和稀硫酸,观察试管口是否有红棕色气体出现 | 检验该无色溶液中是否存在 |
B | 将酒精与碘水在分液漏斗中充分振荡混匀、静置 | 萃取 |
C | 将澄清石灰水滴入可能混有 | 检验是否存在 |
D | 将 | 配制 |
- A、 A
- B、 B
- C、 C
- D、 D
试题详情
M、L、P、Q为四种短周期主族元素,原子序数依次增大。M与L相邻,M基态原子核外有2个未成对电子,P是元素周期表中电负性最大的元素,Q原子在同周期中原子半径最大。下列说法正确的是( )
- A、 M、L、P的第一电离能:
- B、 L、Q的简单离子的半径:
- C、 最高价氧化物对应的水化物的酸性:L<M
- D、
的空间结构为平面三角形
试题详情
硅锰电池是一种新型电池,其工作原理如图所示。下列说法错误的是( )
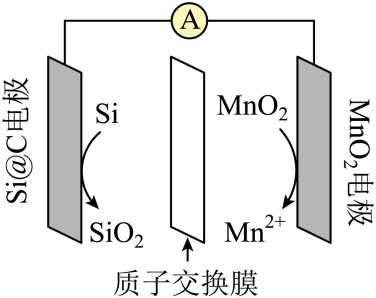
- A、 电池充电时,
电极连接外接电源的正极
- B、 电池工作时,
通过质子交换膜由Si@C电极区移向
电极区
- C、 电池充电时,Si@C电极的电极反应式是
- D、 放电时,导线上每通过0.2mol电子,正极区溶液的质量增加8.7g
试题详情
25℃时,用 溶液滴定
溶液滴定 溶液,加入NaOH溶液的体积、
溶液,加入NaOH溶液的体积、 与pH的变化关系如图所示。下列说法正确的是( )
与pH的变化关系如图所示。下列说法正确的是( )
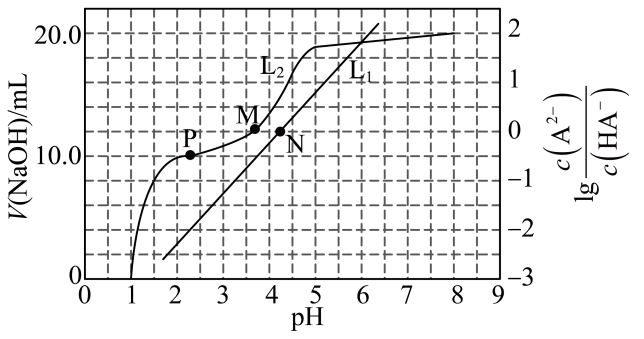
- A、
表示加入NaOH溶液的体积与pH的变化关系
- B、
的第二步电离常数
的数量级为
- C、 M点所处溶液中:
- D、 第二滴定终点可以选择甲基橙做指示剂
非选择题(本大题共4小题,共58分)
试题详情
Ⅰ.已知25℃时部分弱电解质的电离平衡常数如下表所示,请回答下列问题:
化学式 | |||||
电离常数 |
试题详情
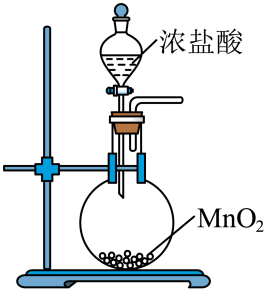
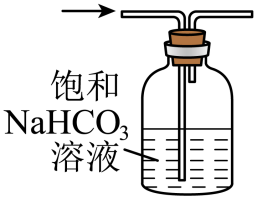
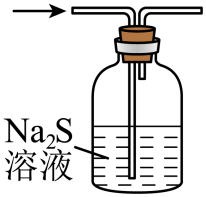
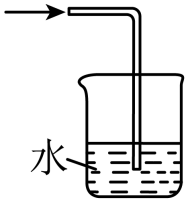
硫氰化钾主要用于合成树脂、杀虫杀菌剂等,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如下图所示:
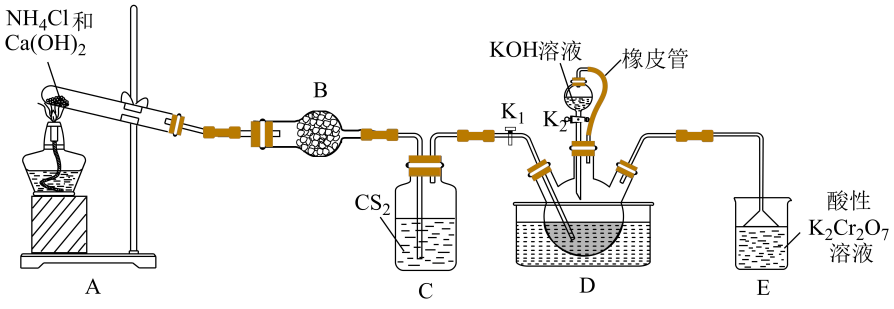
已知:①不溶于
,
密度比水大且不溶于水;
②三颈烧瓶内盛放:、水和催化剂;
③ , 该反应比较缓慢且
在高于170℃易分解。
回答下列问题:
试题详情  和ZnO都是常用的化学添加剂,一种以含锌废液(主要含有
和ZnO都是常用的化学添加剂,一种以含锌废液(主要含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 )为原料,制备
)为原料,制备 和ZnO的工艺流程如下:
和ZnO的工艺流程如下:

已知:常温下,、
,
、
开始沉淀至完全沉淀时的pH分别为2.7~3.7、4.2~5.1、5.4~6.7、6.2~8.0。回答下列问题:
试题详情
我国力争2030年前实现碳达峰, 的捕集、利用已成为科学家研究的热点。
的捕集、利用已成为科学家研究的热点。 在固体催化剂表面加氢合成甲烷过程中发生如下反应:
在固体催化剂表面加氢合成甲烷过程中发生如下反应:
主反应Ⅰ:
副反应Ⅱ:

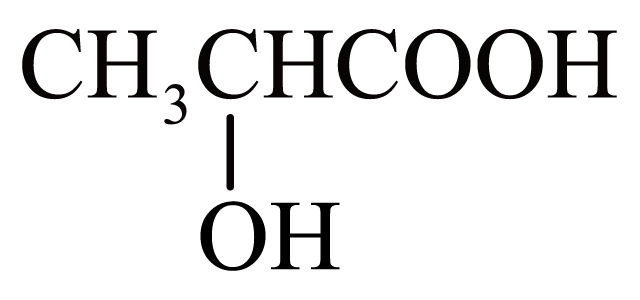 )分子中含有1个手性碳原子
)分子中含有1个手性碳原子