单选题
- A、 航天服壳体使用的铝合金材料熔点比纯铝高
- B、 打印机墨粉中常加有Fe3O4 , 这是利用了其颜色和磁性特点,可用CuO替代Fe3O4
- C、 华为5G手机芯片的主要成分是二氧化硅
- D、 中国天眼FAST用到的高性能碳化硅是一种新型的无机非金属材料
- A、 ClO2具有强氧化性,可用于消毒杀菌
- B、 浓硫酸具有脱水性,可用于干燥气体
- C、 铝具有良好导热性,可用铝罐贮运浓硝酸
- D、 FeCl3溶液具有酸性,可用作铜制线路板的蚀刻剂
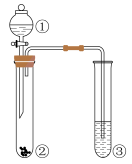
- A、 若②中为
固体,③中盛石蕊溶液,则③中溶液先变红后褪色
- B、 若②中为蔗糖,③中盛有溴水,能说明浓硫酸具有脱水性和氧化性
- C、 若②中为
固体,③中盛有氯化钡溶液,则③中生成白色沉淀
- D、 若②中为铜单质,③中盛有硫化氢水溶液,则③中生成黄色沉淀
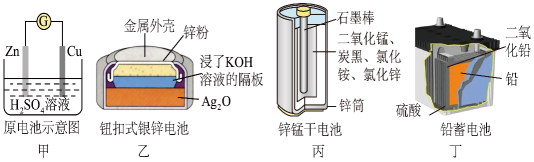
- A、 乙:正极的电极反应式为Ag2O+2e-+H2O=2Ag+2OH-
- B、 甲:溶液中Zn2+向Cu电极方向移动,电子由锌经电解质溶液流向铜电极
- C、 丁:使用一段时间后,电解质溶液的酸性减弱,导电能力下降
- D、 丙:锌筒作负极,发生氧化反应,锌筒会变薄

- A、 电流从左侧电极经过负载后流向右侧电极
- B、 电极A极反应式为
- C、 为使电池持续放电,离子交换膜需选用阴离子交换膜
- D、 当有
被处理时,转移电子数为

下列说法错误的是( )
- A、 在该过程中,CO断键形成C和O
- B、 CO和O生成了具有极性共价键的CO2
- C、 CO和O生成CO2是放热反应
- D、 催化剂可加快该反应的速率
- A、 通入甲烷的电极为正极
- B、 电池工作一段时间后,溶液的碱性增强
- C、 负极的电极反应:CH4+l0OH﹣﹣8e﹣=CO32﹣+7H2O
- D、 通入甲烷的电极的电极反应:O2+2H2O+4e﹣=4OH﹣
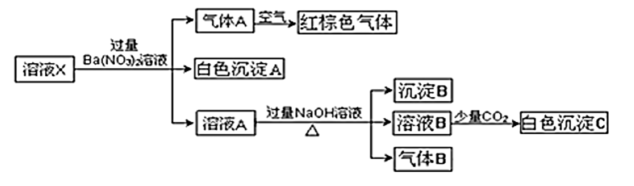
- A、 原溶液中一定存在NH
、Fe2+、SO
- B、 原溶液中可能含有NO
和Al3+
- C、 白色沉淀C可能是Al(OH)3
- D、 沉淀B可能是Fe(OH)2和Fe(OH)3的混合物

- A、 该反应达到平衡状态的时间是
- B、 用Y表示
内该反应的平均速率为
- C、 第
末,X的转化率为90%
- D、 该反应的化学方程式为
- A、 加入NH4HS固体
- B、 压强、温度不变,充入少量氩气
- C、 容积、温度一定,充入氦气
- D、 温度、容积一定,充入H2S气体

- A、 图1所示反应:X(g) +Y(g)
2Z(g),曲线b一定是增大了反应体系的压强。
- B、 图2 表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂
- C、 图3 表示向Ca(HCO3)2溶液中滴入NaOH溶液所得沉淀的质最变化
- D、 图4 表示明矾溶液受热时氢氧根离子浓度随温度的变化

- A、 a为阳离子交换膜、b为阴离子交换膜
- B、 电子由Zn电极经过外电路流向
电极
- C、 放电时,Zn电极反应为
- D、 消耗6.5gZn的同时,
电极理论上应增重3.2g
随时间变化的有关实验数据见下表:
时间/min | 0 | 2 | 4 | 6 | 8 | 10 |
200℃ | 1.60 | 1.10 | 0.70 | 0.40 | 0.30 | 0.30 |
t℃ | 2.00 | 1.30 | 0.70 | 0.36 | 0.36 | 0.36 |
下列有关该反应的描述正确的是( )
- A、 在200℃时,4 min内用Y表示的化学反应速率为
- B、 t℃下,6 min时反应刚好达到平衡状态
- C、 根据上表内X的浓度变化,可知浓度越大,反应速率越大
- D、 从表中可以看出

- A、 反应开始2分钟内平均反应速率最大
- B、 反应4分钟后平均反应速率最小
- C、 反应开始4分钟内温度对反应速率的影响比浓度大
- D、 反应4分钟后反应速率下降的原因是盐酸浓度逐渐减小
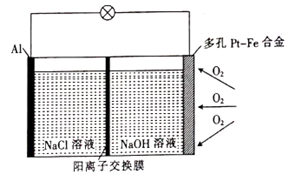
- A、 多孔Pt—Fe合金电极有利于吸附O2
- B、 负极的电极反应式为
- C、 若反应中消耗5.4 g Al,则消耗3.36 L O2
- D、 当1 mol O2参与反应时,有4 mol阳离子通过阳离子交换膜
填空题
某小组同学欲探究NH3催化氧化反应,按下图装置进行实验.
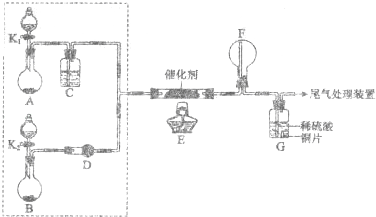
A、B装置可选药品:浓氨水、H2O2、蒸馏水、NaOH固体、MnO2
(1)NH3催化氧化的化学方程式是 ;
(2)装置B中产生气体的原因有(结合化学用语解释) ;
(3)甲乙两同学分别按上述装置进行实验.一段时间后,装置G中溶液都变成蓝色.
①甲观察到装置F中有红棕色气体,生成红棕色气体的化学方程式是 ;
②乙观察到装置F中只有白烟生成,白烟的成分是(写化学式) ;
③用离子方程式解释装置G中溶液变成蓝色的原因: ;
(4)为帮助乙实现在装置F中也观察到红棕色气体,可在原实验的基础上进行改进.
①甲认为可调节K1和K2控制A、B装置中的产气量,应(填“增加”或“减少”) 装置A中的产气量,或(填“增加”或“减少”) 装置B中的产气量.
②乙认为可在装置E、F间增加一个装置,该装置可以是(填序号)

(1)下列反应属于吸热反应的是
A.C6H12O6(葡萄糖)+6O2═6CO2+6H2O
B.CH3COOH+KOH═CH3COOK+H2O
C.大多数化合反应
D.破坏生成物全部化学键所需能量小于破坏反应物全部化学键的能量
E.Ba(OH)2•8H2O晶体与NH4Cl晶体反应
F.金属与酸或水的反应
(2)在一定温度下的定容密闭容器中,发生反应:A(s)+2B(g)⇌C(g)+D(g),能表明反应已达平衡状态的是
A.混合气体的压强不变
B.混合气体的密度不变
C.单位时间内生成n molC的同时生成n mol D
D.气体总物质的量不变
E.A的物质的量不再变化
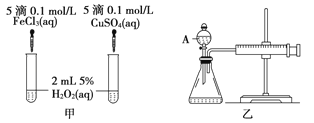
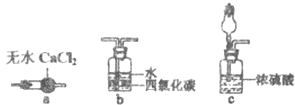
(3)经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验.回答相关问题:
①定性分析:如图甲可通过观察 来定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是
②定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略.图中仪器A的名称为 ,实验中需要测量的数据是 .检查乙装置气密性的方法是 .